王少華*,劉姝晶
(國家知識產權局專利局, 北京 100088)
[ 摘要] 鈉-葡萄糖協同轉運蛋白(SGLT)抑制劑是治療2 型糖尿病的新型藥物,簡介SGLT 抑制劑的作用機制和研發現狀,重點分析SGLT抑制劑在中國的專利申請量、申請人、技術領域、重點公司等。通過比較國外申請人和國內申請人在專利技術方面的優勢和劣勢,為國內SGLT 抑制劑的深入開發提供參考。
糖尿病是嚴重威脅人類健康的世界性公共衛生問題。隨著人口老齡化以及肥胖發生率的增加,糖尿病的發病率呈逐年上升趨勢,世界各地的糖尿病患者中有90% 為2 型糖尿病 。目前2 型糖尿病治療藥物的作用機制主要集中于增加胰島素釋放、增加胰島素敏感性、抑制腸道吸收葡萄糖等,但是伴隨著許多與藥物相關的不良反應,如體質量增加、胰島素分泌減少、低血糖、胃腸道不良反應等。因此,2 型糖尿病的藥物治療仍然是一個世界性難題,尋找和開發新型作用機制、毒副作用小的治療藥物,已成為學術界和醫藥工業界共同關注和亟待解決的熱點問題。目前研究發現,通過抑制腎臟葡萄糖重吸收、增加葡萄糖排出可有效降低血糖,與之相關的鈉-葡萄糖協同轉運蛋白(SGLT)抑制劑成為抗糖尿病研發的新靶點藥物。
1 SGLT 抑制劑作用機制
健康成人每天約有180 g 的葡萄糖從腎小球濾過,但正常的腎臟僅通過尿液每天排出500 mg 葡萄糖,其余的均被重吸收。葡萄糖經腎小球濾過,90% 的葡萄糖通過SGLT2 在近曲小管S1 段被重吸收,其余10%通過SGLT1 在近曲小管遠端的S3 段被重吸收。可見,SGLT2 在葡萄糖的重吸收中起主導作用,通過阻斷SGLT,尤其是SGLT2,可減少近曲小管對葡萄糖的重吸收,排出多余的糖,從而降低血糖。SGLT2 抑制劑治療糖尿病******的優勢是不引起低血糖。
2 SGLT 抑制劑研發現狀
自2012 年歐盟委員會批準首個SGLT2 抑制劑達格列凈用于成人2 型糖尿病患者的治療,目前國外共有6 個SGLT2 抑制劑單方藥物上市,分別為:強生、三菱制藥的卡格列凈(canagliflozin,或稱坎格列凈);阿斯利康的達格列凈(dapagliflozin);勃林格殷格翰、禮來的恩格列凈(empagliflozin,或稱艾格列凈);安斯泰來、日本壽制藥的伊格列凈(ipragliflozin,或稱依格列凈);大正制藥的魯格列凈(luseogliflozin) 以及Chugai、Sanofi、Kowa 公司的托格列凈(tofogliflozin)。前3 種獲美國FDA 批準,后3 種獲日本厚生勞動省批準。中國國家食品藥品監督管理總局(CFDA)于2017 年正式批準上市的首個SGLT2 抑制劑是阿斯利康公司的新藥達格列凈,可作為單藥用于改善2 型糖尿病成人患者的血糖控制。目前國內有很多大型藥企投入巨資研究SGLT2抑制劑,已有多個新藥進入Ⅰ、Ⅱ期臨床研究階段。如何順應國際上SGLT2 抑制劑發展趨勢,抓住發展機會,提早進行專利布局,突破跨國醫藥巨頭的專利封鎖,在潛力巨大的糖尿病治療藥物市場中占有一席之地,是國內藥企急需解決的難題。
3 SGLT 抑制劑的專利分析
在中國專利數據庫(CNPAT)中,以“SGLT”為關鍵詞,對涉及SGLT 的專利申請進行檢索,共檢索到178 件專利申請,截止日期是2016 年12 月26 日。通過對SGLT 抑制劑的中國專利申請量、申請人、分類號、重要申請人進行分析,研究國外主要專利權人在SGLT 抑制劑領域的專利布局,與國內該領域專利技術分布進行對比,客觀分析我國在SGLT 抑制劑領域存在的技術優勢和劣勢,提出專利布局和產業發展方面的建議,以促進我國SGLT 抑制劑相關行業的發展。
3.1 申請量
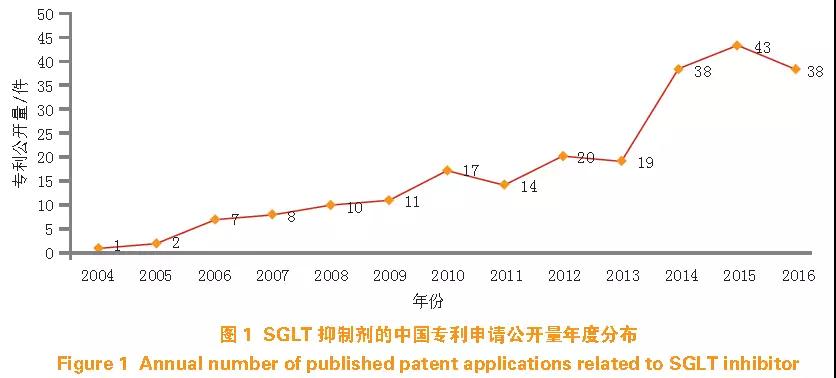
圖1 顯示了最近12 年國內SGLT 抑制劑的專利申請公開量。2004—2016 年,國內總共公開了178 件SGLT 抑制劑的專利申請。在2008 年以前,SGLT 抑制劑的專利申請公開量均為個位數,2008 年以后,專利申請公開量逐年增長,到2015 年,專利申請公開量達到高峰,為43 件。可見SGLT 抑制劑在國內的專利申請量有逐漸增加的趨勢。其中2016 年之后的專利申請數量有所下降,則是由于很多專利未公開導致(國內專利申請滿18 個月公開,國外專利大多通過PCT 途徑進入我國,從申請到公開周期超過32 個月),數據有低估的可能性。總的來看,國內關于SGLT 的研究處于技術發展期。
3.2 申請人
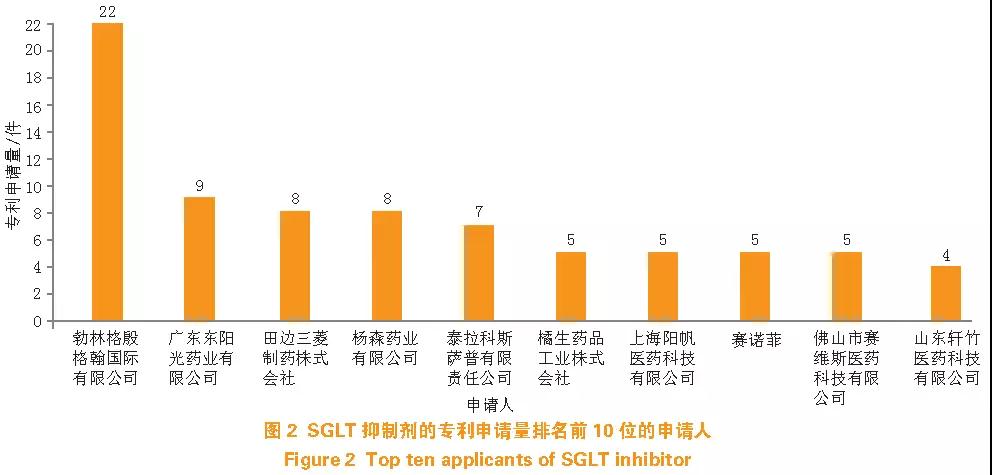
圖2 顯示,排名前10 位的專利申請人中有6 個國外申請人,可見SGLT 抑制劑專利申請主要為國外申請,申請量最高的申請人勃林格殷格翰國際有限公司(德國)為國外申請人,顯示出跨國制藥公司在SGLT 研發領域有很強優勢。
排名前10 位的申請人中國內申請人僅有4 位,分別是:廣東東陽光藥業有限公司、上海陽帆醫藥科技有限公司、佛山市賽維斯醫藥科技有限公司和山東軒竹醫藥科技有限公司,且國內申請人的申請總量不高,顯示我國SGLT 制藥領域的研發還處于起步階段。
3.3 分類號
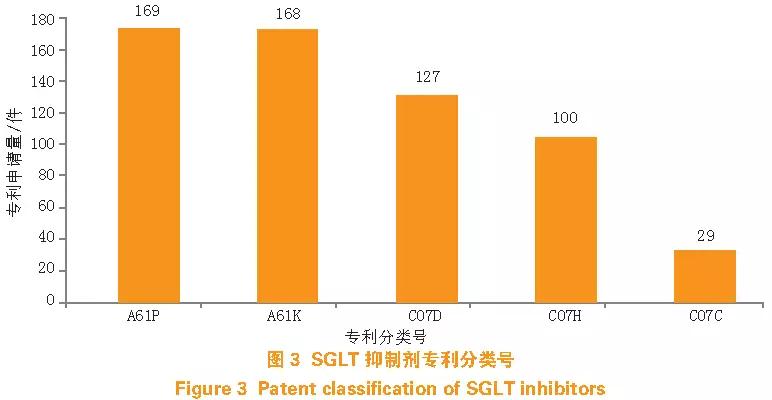
由于1 件專利申請可以有幾個分類號,因此,對重點技術分析時不但要考慮主分類號,還要考慮副分類號,按照每個IPC 專利分類計數(即如果1 個專利有3 個分類號,記為3 件專利)。對178 件SGLT 抑制劑專利的分類號進行分析顯示,這些分類號涉及1)A61K:醫用、牙科用或梳妝用的配制品;2)A61P:化合物或藥物制劑的特定治療活性;3)C07D:雜環化合物;4)C07H:糖類及其衍生物、核苷、核苷酸、核酸;5)C07C:無環或碳環化合物。從化合物采用的分類號來看,SGLT 抑制劑的結構主要為雜環化合物,其次為糖類衍生物,再次為無環或碳環化合物(見圖3)。世界上首個被發現的SGLT 抑制劑是根皮苷,從分類號上來看其屬于C07H。現有C07H 分類號的SGLT 抑制劑專利申請也多為根皮苷的衍生物。
3.4 重要專利申請人專利申請分析
3.4.1 勃林格殷格翰國際有限公司
勃林格殷格翰國際有限公司是國外SGLT2 抑制劑的主要研發公司。作為目前國際上已上市的6 種SGLT2 抑制劑之一的恩格列凈最初就是由勃林格殷格翰獨立研發的,后與禮來公司聯合開發。恩格列凈的優勢在于不僅能降低血糖,且能降低心血管疾病死亡的風險,是美國FDA 批準的首個用于降低2 型糖尿病合并心血管疾病成人患者的心血管死亡風險的SGLT2 抑制劑 。糖尿病患者心血管事件病死率是未患糖尿病者的1.7 倍 ,恩格列凈為2型糖尿病合并心血管疾病的成人患者的治療帶來希望,具有廣闊的市場前景。
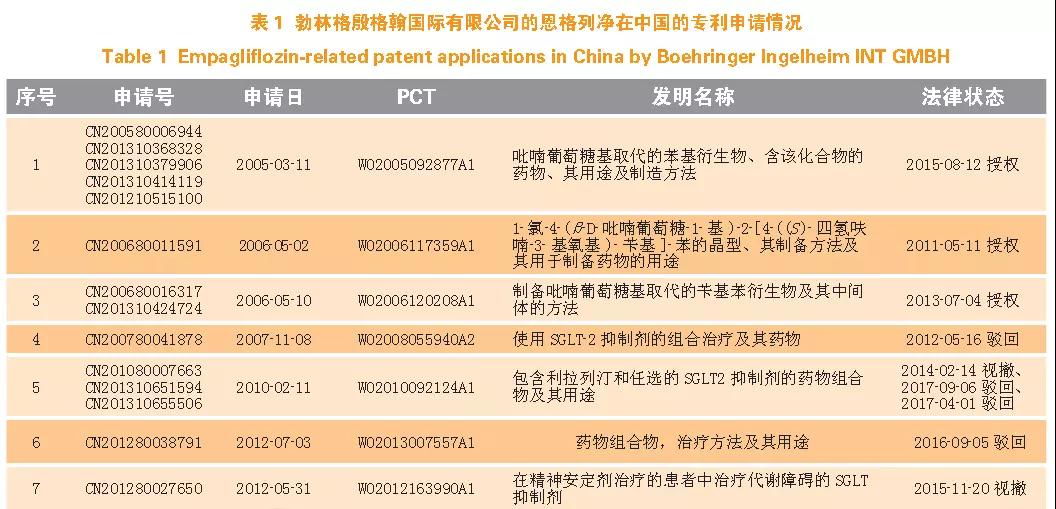
在SGLT 抑制劑專利申請中,以勃林格殷格翰國際有限公司為申請人,共檢索到22 件專利申請(同族專利記為1 件),其中7 件屬于恩格列凈專利(見表1)。
在化合物專利方面,勃林格殷格翰國際有限公司的恩格列凈化合物專利于2005 年申請了PCT 國際申請,這件PCT 國際申請是恩格列凈的基礎專利,公開號是WO2005092877A1, 進入中國的申請號是CN200580006944,后又分案申請了4 件專利申請。該專利采用馬庫什通式進行撰寫,取代基范圍廣泛,從而涵蓋了一系列具有相同根皮苷母核結構的化合物,對后來者形成了一定的專利壁壘。該化合物專利直到2015 年才在中國獲得授權,授權的權利要求僅保護了恩格列凈及其對應異構體和相關藥物組合物、制藥用途等。原因是最初要求保護的通式化合物與在先公開的達格列凈區別僅在于部分取代基不同,刪除與達格列凈結構相近的化合物后才獲得授權,授權的權利要求保護范圍大大縮小。
在外圍專利方面,從2006 年起,勃林格殷格翰國際有限公司在恩格列凈的晶型專利(WO2006117359A1)和制備方法專利(WO2006120208A1)方面就已開始布局,且在中國獲得授權。之后恩格列凈的專利保護重點在聯合用藥方面,WO2008055940A2 要求保護和二甲雙胍等的聯合用藥,WO2010092124A1 要求保護和利格列汀的聯合用藥。但由于最早的恩格列凈化合物專利CN200580006944 已經公開了和二甲雙胍等的聯合用藥,因而WO2008055940A2 的中國申請CN200780041878 被駁回。WO2010092124A1 的中國申請均為駁回狀態。WO2013007557A1 要求保護在腎損傷如腎病中的應用,其中國申請處于駁回狀態,WO2012163990A1要求保護因精神安定劑治療誘發的代謝障礙,其中國申請處于視撤狀態。
從與聯合用藥對應的上市藥物來看,美國FDA 在2015 年1 月批準勃林格殷格翰公司的糖尿病復方藥物Glyxambi,這款復方藥物由SGLT2 抑制劑恩格列凈與DPP-4 抑制劑利格列汀組成,與來自阿斯利康、強生/Tanabe 及輝瑞/默沙東的產品展開競爭。美國FDA在2015 年9 月批準勃林格殷格翰的糖尿病復方藥物Synjardy,該復方藥物與FDA 在2013 年8 月批準的強生公司的Invokamet 和2014 年10 月批準的阿斯利康的Xigduo 展開競爭。勃林格殷格翰這2 款已上市復方藥物的專利在中國未獲得授權,為中國的仿制藥企業在該領域的開發留下一定空間。
從上述專利分析來看,勃林格殷格翰公司的專利保護具有以下特點:1)專利布局全面,形成有效專利壁壘。從化合物的基礎專利開始布局,圍繞化合物專利,進行了制備方法、晶型專利、聯合用藥專利的布局。勃林格殷格翰公司是最早在中國進行該藥晶型專利申請的制藥公司之一。同時,該公司還不斷對恩格列凈的結構進行改進,申請了對恩格列凈化合物的取代基進行一些基團替換的專利。從授權前景來看,僅僅進行常規基團替換獲得的新化合物可能會因為不具有創造性而無法獲得授權,這種專利上的不確定性不利于具有上市前景的藥物的保護。為了獲得授權的產品專利,勃林格殷格翰公司提早進行了這些新化合物的晶型專利和聯合用藥專利布局,為未來可能進入市場的藥物保駕護航。2)與其他醫藥巨頭聯合開發。除了恩格列凈是與禮來公司聯合開發之外,還有2 件專利是與味之素株式會社合作申請,要求保護的是一種新的具有吡唑基取代的SGLT2 抑制劑。
3.4.2 廣東東陽光藥業有限公司
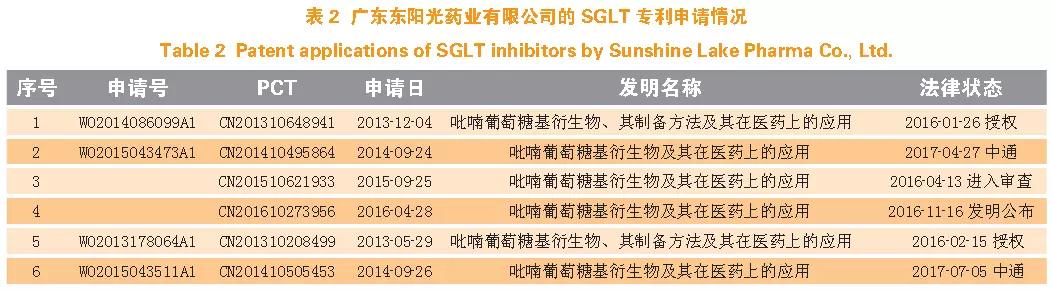
廣東東陽光藥業有限公司是國內新藥研發走在前列的公司之一,近年來申請了眾多的新藥專利。廣東東陽光藥業有限公司曾申請多件PCT 國際專利,有的專利申請顯示其在某些藥物研發領域緊跟國際研發前沿技術,有良好的發展前景。廣東東陽光的SGLT 抑制劑專利申請要求保護的化合物是在達格列凈的基礎上進行的結構改造,即在達格列凈化合物的吡喃糖環上增加了橋環或螺環,其重要專利如表2 所示。
從上述專利分析來看,廣東東陽光在SGLT 抑制劑領域的研發具有以下特點:1)對于SGLT 抑制劑的開發時間晚,全部專利的申請日在2013 年之后。2)專利布局不完善,化合物專利之后并未緊跟著申請化合物的晶型專利、復合物專利。3)化合物專利雖然巧妙避開已有專利獲得授權,但仍屬于在已有上市藥物基礎上的結構改進,未發現全新結構。4)未同時進行心血管疾病方面研究,不明確是否能夠同時作為SGLT2 抑制劑和防治心血管疾病藥物。5)均為單一申請人,未進行聯合申請。
4 SGLT 抑制劑專利分析的啟示
4.1 進行全面專利布局
從中國專利申請狀況來看,國外申請人已經開始在中國對于SGLT 抑制劑進行專利布局,且專利布局比較全面。由國外公司的專利申請實踐來看,圍繞化合物專利,進行其晶型、化合物制備方法、復方藥物專利申請進行保護,能夠延長藥物的保護期限。國內的藥企在專利布局方面還有待完善,政府相關部門可以在專利分析、專利申請、專利保護等各個方面進行支持。
4.2 挖掘有價值專利
國外醫藥巨頭圍繞SGLT 抑制劑的化合物專利進行了外圍專利申請,包括晶型專利、復方藥物專利等。但是,從國內授權情況來看,這些外圍專利申請很多并沒有在中國獲得授權,尤其是國外已上市的復方藥物,在國內沒有專利授權,這為我國藥企在本領域的市場發展留下了一定空間。
4.3 聯合開發是主要趨勢
國際上已上市的6 個SGLT 藥物中,有4 個是幾大醫藥巨頭聯合開發。藥物開發的巨大投入迫使跨國醫藥巨頭都使用聯合開發的手段。作為國內藥企,盡管起步晚、技術落后、規模小,但為在糖尿病藥物市場占有一席之地,更需要借助各種手段趕上醫藥發展的浪潮。由于SGLT 抑制劑的藥物研發耗資巨大,且周期長,單單依靠國內單一的研究組織難以完成新藥從研發到上市的漫長過程。因此進行國際合作、借助跨國藥企或國外大學、研究機構的技術優勢是目前藥物研發的新趨勢。聯合開發的具體方式包括:項目引進,例如可以選擇國外已經研發到一定程度的SGLT 新藥進行合作開發;還可以進行項目轉讓以及合資與并購等,例如廣東東陽光已經獲得專利授權的幾個SGLT 抑制劑有很好的市場前景,通過合作或技術引進等可以加快上市步伐。通過多種形式的國際合作,縮短與發達國家研發水平的差距,爭取早日使得我國自主生產的SGLT 抑制劑藥物進入臨床應用。
文章轉自《藥學進展》